







**为什么这本指南是RAC Devices考生与国际注册从业者的首选?**
作为全球医疗器械事务领域的核心参考书,本书系统梳理从产品概念设计到退市管理的完整合规路径,深度契合RAC Devices认证考试能力模型,同时直击企业实际注册申报痛点。
**全面覆盖全球医疗器械全流程**
内容贯穿器械全生命周期:研发阶段的设计控制与风险管理、临床评价策略与试验合规要点、技术文档(Technical File / Design Dossier)编制规范、各国市场准入路径选择,以及上市后监督(PMS)、UDI实施、警戒报告与产品召回等关键环节。
**精准对接2025年RAC Devices考试最新要求**
严格依据RAC-Devices®考试蓝图(2025版)编排章节,涵盖FDA 510(k)、PMA与De Novo分类路径详解、欧盟MDR/IVDR重大修订解读、全球主要机构(如FDA、EMA、Health Canada、TGA、MHLW/PMDA)职能与协作机制等内容,确保学习内容零偏差。
**聚焦高价值实务模块,即学即用**
• 全球医疗器械体系架构与区域差异分析
• 器械分类规则与风险等级判定方法论
• 设计开发过程中的设计控制(Design Control)实施要点
• 临床证据构建逻辑:等效性论证、文献评估与临床试验豁免条件
• FDA与欧盟注册资料核心要素对比及常见缺陷解析
• ISO 13485质量管理体系与符合性融合实践
• UDI编码规则、EUDAMED数据库对接、不良事件监测(MAUDE/EudraVigilance)操作指南
**2025新版PDF专属优势**
✓ 同步更新至2025年Q1全球动态(含MDR过渡期延长政策、FDA AI/ML软件新规、IVDR体外诊断分类调整)
✓ 高清可检索PDF格式,支持关键词定位、笔记标注与跨设备同步阅读
✓ 中英术语对照+关键原文索引,兼顾专业性与实操性
✓ 适用于医疗器械企业事务、注册申报、质量保证、临床运营及合规审计等多岗位人员






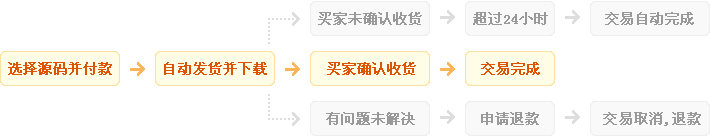
发货方式
自动:在特色服务中标有自动发货的商品,拍下后,源码类 软件类 商品会在订单详情页显示来自卖家的商品下载链接,点卡类 商品会在订单详情直接显示卡号密码。
手动:未标有自动发货的的商品,付款后,商品卖家会收到平台的手机短信、邮件提醒,卖家会尽快为您发货,如卖家长时间未发货,买家也可通过订单上的QQ或电话主动联系卖家。
退款说明
1、源码类:商品详情(含标题)与实际源码不一致的(例:描述PHP实际为ASP、描述的功能实际缺少、功能不能正常使用等)!有演示站时,与实际源码不一致的(但描述中有"不保证完全一样、可能有少许偏差"类似显著公告的除外);
2、营销推广类:未达到卖家描述标准的;
3、点卡软件类:所售点卡软件无法使用的;
3、发货:手动发货商品,在卖家未发货前就申请了退款的;
4、服务:卖家不提供承诺的售后服务的;(双方提前有商定和描述中有显著声明的除外)
5、其他:如商品或服务有质量方面的硬性常规问题的。未符合详情及卖家承诺的。
注:符合上述任一情况的,均支持退款,但卖家予以积极解决问题则除外。交易中的商品,卖家无法修改描述!
注意事项
1、在付款前,双方在QQ上所商定的内容,也是纠纷评判依据(商定与商品描述冲突时,以商定为准);
2、源码商品,同时有网站演示与商品详情图片演示,且网站演示与商品详情图片演示不一致的,默认按商品详情图片演示作为纠纷评判依据(卖家有特别声明或有额外商定的除外);
3、点卡软件商品,默认按商品详情作为纠纷评判依据(特别声明或有商定除外);
4、营销推广商品,默认按商品详情作为纠纷评判依据(特别声明或有商定除外);
5、在有"正当退款原因和依据"的前提下,写有"一旦售出,概不支持退款"等类似的声明,视为无效声明;
6、虽然交易产生纠纷的几率很小,卖家也肯定会给买家最完善的服务!但请买卖双方尽量保留如聊天记录这样的重要信息,以防产生纠纷时便于送码网快速介入处理。
亿万码声明
1、作为第三方中介平台,依据双方交易合同(商品描述、交易前商定的内容)来保障交易的安全及买卖双方的权益;
2、平台上所有的资源都是亲测无误的,在平台下单安全有保障,有任何问题,可以随时联系在线客服。